Rezdiffra (resmetirom) je odobrena od strane FDA iz SAD-a za liječenje odraslih osoba s necirotičnim bezalkoholnim steatohepatitisom (NASH) s umjerenim do uznapredovalim ožiljcima na jetri (fibrozom), za korištenje uz dijetu i tjelovježbu.
Do sada pacijenti s necirotičnim bezalkoholnim steatohepatitisom (NASH) koji također imaju značajne ožiljke na jetri nisu imali lijek koji bi mogao izravno utjecati na njihovu oštećenje jetre. FDA-e approval of Rezdiffra will, for the first time, provide a liječenje option for these patients, in addition to diet and exercise.
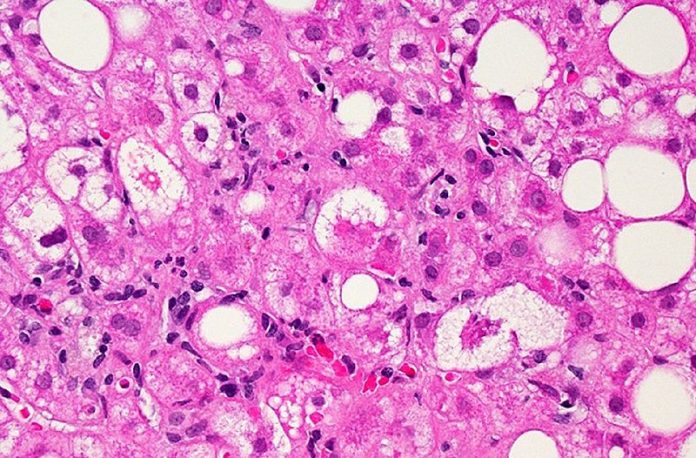
NASH is a result of the progression of non-alcoholic fatty jetra bolest gdje jetra inflammation, over time, can lead to liver scarring and liver dysfunction. NASH is often associated with other health problems such as high blood pressure and type 2 diabetes. By at least one estimate, approximately 6-8 million people in the U.S. have NASH with moderate to advanced liver scarring, with that number expected to increase.
Rezdiffra je djelomični aktivator receptora hormona štitnjače; aktivacija ovog receptora pomoću Rezdiffre u jetri smanjuje nakupljanje masti u jetri.
Sigurnost i djelotvornost lijeka Rezdiffra
The safety and efficacy of Rezdiffra was evaluated based on an analysis of a surrogate endpoint at month 12 in a 54-month, randomized, double-blind placebo-controlled trial. The surrogate endpoint measured the extent of jetra inflammation and scarring. The sponsor is required to conduct a postapproval study to verify and describe Rezdiffra’s clinical benefit, which will be done through completing the same 54-month study, which is still ongoing. To enroll in the trial, patients needed to have a jetra biopsy showing inflammation due to NASH with moderate or advanced jetra scarring. In the trial, 888 subjects were randomly assigned to receive one of the following: placebo (294 subjects); 80 milligrams of Rezdiffra (298 subjects); or 100 milligrams of Rezdiffra (296 subjects); once daily, in addition to standard care for NASH, which includes counseling for healthy diet and exercise.
At 12 months, liver biopsies showed that a greater proportion of subjects who were treated with Rezdiffra achieved NASH resolution or an improvement in liver scarring as compared with those who received the placebo. A total of 26% to 27% of subjects who received 80 milligrams of Rezdiffra and 24% to 36% of subjects who received 100 milligrams of Rezdiffra experienced NASH resolution and no worsening of liver scarring, compared to 9% to 13% of those who received placebo and counseling on diet and exercise. The range of responses reflects different pathologists’ readings. In addition, a total of 23% of subjects who received 80 milligrams of Rezdiffra and 24% to 28% of subjects who received 100 milligrams of Rezdiffra experienced an improvement in jetra scarring and no worsening of NASH, compared to 13% to 15% of those who received placebo, depending on each pathologist’s readings. Demonstration of these changes in a proportion of patients after just one year of treatment is notable, as the bolest typically progresses slowly with most patients taking years or even decades to show progression.
Nuspojave Rezdiffre
Najčešće nuspojave Rezdiffre uključivale su proljev i mučninu. Rezdiffra dolazi s određenim upozorenjima i mjerama opreza, kao što su toksičnost jetre uzrokovana lijekovima i nuspojave povezane sa žučnim mjehurom.
Use of Rezdiffra should be avoided in patients with decompensated cirrhosis. Patients should stop using Rezdiffra if they develop signs or symptoms of worsening jetra function while on Rezdiffra treatment.
Interakcije lijekova Rezdiffre
Primjena Rezdiffre u isto vrijeme s određenim drugim lijekovima, posebice statinima za snižavanje kolesterola, može dovesti do potencijalno značajnih interakcija lijekova. Pružatelji zdravstvenih usluga trebali bi pogledati sve informacije o propisivanju za dodatne informacije o ovim potencijalno značajnim interakcijama lijekova s Rezdiffrom, preporučenom doziranju i izmjenama primjene.
Korištenje električnih romobila ističe FDA approved Rezdiffra under the accelerated approval pathway, which allows for earlier approval of drugs that treat serious conditions and address an unmet medical need, based on a surrogate or intermediate clinical endpoint that is reasonably likely to predict clinical benefit. The required aforementioned 54-month study, which is ongoing, will assess clinical benefit after 54 months of Rezdiffra treatment.
Rezdiffra je dobila oznake Breakthrough Therapy, Fast Track i Priority Review za ovu indikaciju.
Korištenje električnih romobila ističe FDA granted the approval of Rezdiffra to Madrigal Pharmaceuticals.
***
Izvor:
FDA 2024. Objava za vijesti – FDA odobrava prvi tretman za pacijente s ožiljcima na jetri zbog masne bolesti jetre. Objavljeno 14. ožujka 2024. Dostupno na https://www.fda.gov/news-events/press-announcements/fda-approves-first-treatment-patients-liver-scarring-due-fatty-liver-disease
***